神经胶质瘤(Glioma)是最常见的原发性中枢神经系统肿瘤,其源于神经胶质细胞的癌变,肿瘤细胞生长速度快,浸润性破坏脑组织,造成一系列的症状,如偏瘫、头痛、呕吐、意识障碍等。其中恶性胶质瘤是肿瘤中生存期最短、恶性程度最高的肿瘤之一。由于胶质瘤浸润性生长,与脑组织间无明显边界,当前临床手术治疗难以做到完全切除。随着精准外科理念的提出,术中导航技术逐渐被应用于临床,让外科手术有了“地图”的指引,对于高度浸润的、周围组织复杂的胶质瘤切除手术,具有极大的临床价值。而基于荧光实时成像的荧光引导手术,其荧光分子探针能在术中实时点亮癌细胞,突破了传统手术治疗的精度极限。单胺氧化酶A(Monoamine Oxidase A,MAO-A)的异常表达与胶质瘤的发生发展密切相关,使其成为胶质瘤诊疗的有效靶点。因此,实现胶质瘤中MAO-A的快速、灵敏检测有望应用于肿瘤的早期诊断和术中导航。
近日,厦门大学柔性电子(未来技术)研究院黄维院士、李林教授与西北工业大学彭勃副教授合作在荧光探针领域以“Ultrafast Detection of Monoamine Oxidase A in Live Cells and Clinical Glioma Tissues Using an Affinity Binding-Based Two Photon Fluorogenic Probe”为题,在国际高水平期刊Angew. Chem. Int. Ed.上发表研究性文章(Angew. Chem. Int. Ed. 2023, e202310134)。该工作通过对双光子荧光团进行理性设计,合成出了一种基于亲和力结合的双光子荧光探针(CD1),当CD1进入MAO-A空腔时,空腔内的有限空间限制了包括探针自由旋转在内的构象变化,从而导致荧光信号增强,实现了探针与MAO-A空腔的快速结合。CD1可以在20秒内完成对MAO-A的检测,是目前已知最快的检测MAO-A荧光探针。并且,基于CD1的高敏感性和双光子荧光激发特性,作者成功区分了MAO-A在人脑胶质瘤/瘤旁组织中的表达差异。这些结果证明CD1可作为一种潜在的分子工具,用于在临床快速诊断和术中影像指导胶质瘤切除。
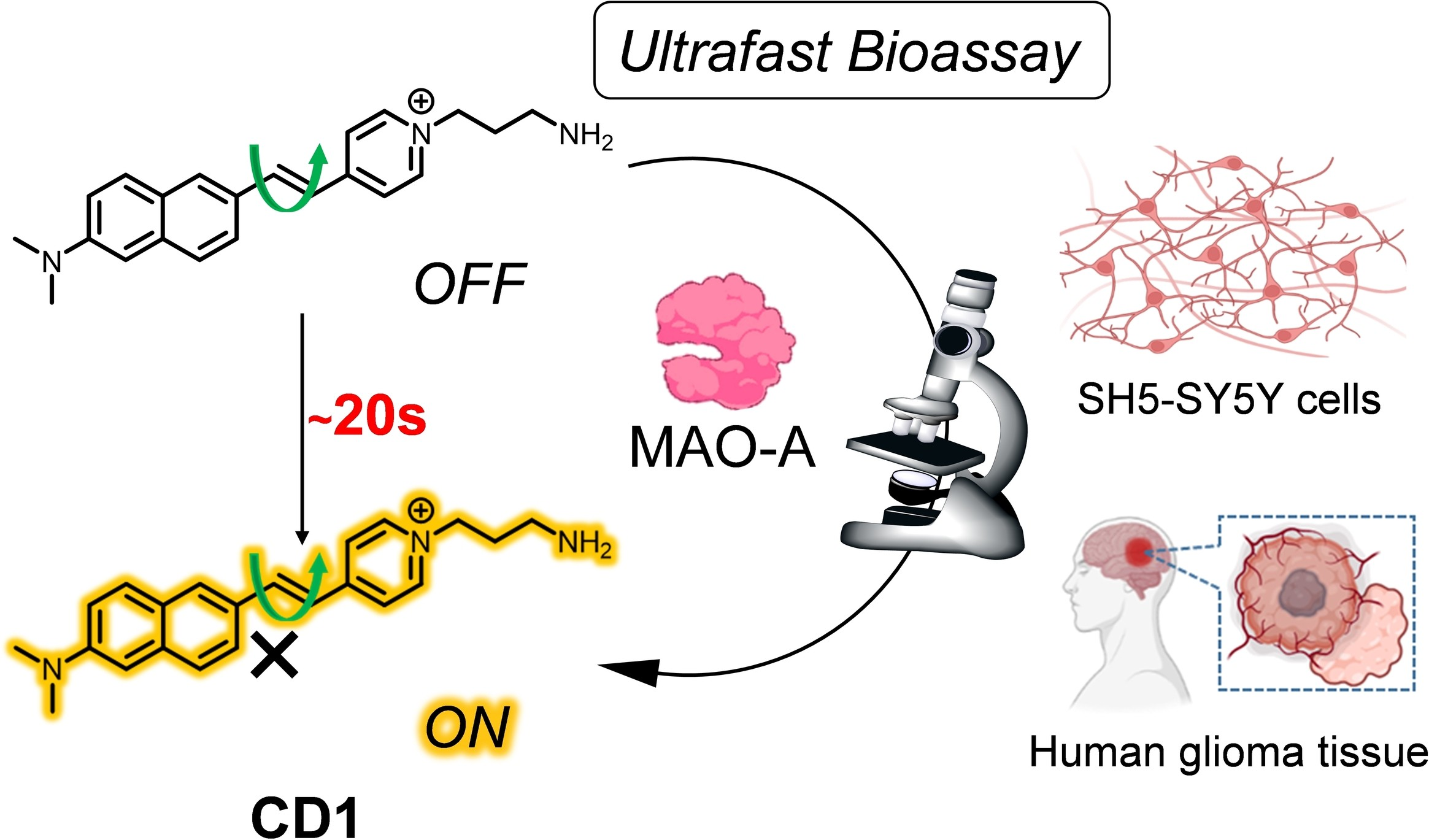
图1 探针快速响应MAO-A以用于神经母胶质瘤细胞和人胶质瘤组织的快速成像
本工作得到了国家重点研发计划、国家自然科学基金等项目的支持。
论文信息:https://doi.org/10.1002/anie.202310134

